Giáo án Hóa học 12 bài Đồng và hợp chất của đồng
Nội dung tài liệu
Tải xuống
Link tài liệu:
Các tài liệu liên quan
-
![Giáo án PTNL Hóa Học lớp 12 (Bản mới)]()
-
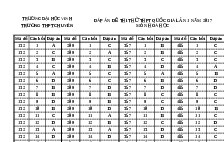
![ĐÁP ÁN đề cương ôn tập môn hóa lớp 12 mã đề 132]()
-
![etylamin va trimetylamin]()
-
![Đề luyện thi THPT Quốc gia năm 2018 môn hóa học (1)]()
-
![GIÁO ÁN HOÁ 12 NC TIẾT 31 KIỂM TRA 1 TIẾT BÀI SỐ 2]()
-
![GIÁO ÁN HOÁ 12 NC TIẾT 30 LUYỆN TẬP POLIME VÀ VẬT LIỆU POLIME]()
-
![GIÁO ÁN HOÁ 12 NC TIẾT 29 VẬT LIỆU POLIME (TIẾT 2)]()
-
![GIÁO ÁN HOÁ 12 NC TIẾT 28 VẬT LIỆU POLIME]()
-
![GIÁO ÁN HOÁ 12 NC TIẾT 27 ĐẠI CƯƠNG VỀ POLIME (TIẾT 2)]()