Bài 39. Benzen
|
Công thức phân tử C6H6 Phân tử khối 78 |
I. TÍNH CHẤT VẬT LÍ
- Benzen C6H6 là chất lỏng, không màu, không tan trong nước, benzen có tính độc. Benzen hòa tan nhiều chất như: dầu ăn, cao su, nến, iot..
II. CẤU TẠO PHÂN TỬ
- Phân tử benzen có cấu tạo là một vòng 6 cạnh, trong đó có ba liên kết đôi xen kẽ với ba liên kết đơn.
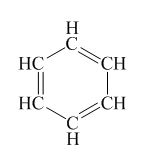 Hoặc
Hoặc 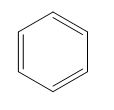
III. TÍNH CHẤT HÓA HỌC
1. Tác dụng với oxi:
- Khi đốt benzen cháy trong không khí tạo ra CO2 và H2O, ngọn lửa có nhiều khói đen (chứa muội than). Nguyên nhân là do phân tử benzen lớn nên khó cháy hoàn toàn thành khí CO2 và hơi nước.
C6H6 + O2 \(\underrightarrow{t^o}\) 6CO2 + 3H2O
2. Phản ứng thế với với brom:
- Benzen không làm mất màu dung dịch brom như etilen và axetilen. Benzen chỉ tham gia phản ứng thế với brom lỏng và cần có xúc tác là bột sắt.
C6H6(l) + Br2(l) \(\underrightarrow{Fe,t^o}\) HBr + C6H5Br (brom benzen)
Chú ý: Benzen chỉ phản ứng với brom nguyên chất không phản ứng với dung dịch nước brom.
3. Phản ứng cộng:
- Benzen khó tham gia phản ứng cộng hơn etilen và axetilen. Tuy nhiên, trong điều kiện thích hợp benzen có phản ứng cộng với một số chất như H2, Cl2,…
C6H6 + H2 \(\underrightarrow{Ni,t^o}\) C6H12 (Xiclohexan)
Kết luận: Do phân tử có cấu tạo đặc biệt nên benzen vừa có phản ứng thế vừa có phản ứng cộng
IV. ỨNG DỤNG
- Benzen là nguyên liệu quan trọng để sản xuất chất dẻo, phẩm nhuộm, dược phẩm, thuốc trừ sâu..
- Benzen làm dung môi hòa tan nhiều chất hữu cơ trong công nghiệp và trong phòng thí nghiệm.




