Đề thi học kì 2 Hóa 8 trường THCS Thái Bình năm 2018-2019
Nội dung tài liệu
Tải xuống
Link tài liệu:
Các tài liệu liên quan
-
![Đề thi học kì 1 Hóa 8 trường THCS TT Vĩnh Tường năm 2017-2018]()
-
![Đề kiểm tra học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa lớp 8 năm 2016-2017]()
-
![Đề thi học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Thái Bình năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Biên Giới năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Sơn Lâm năm 2021-2022]()
-
![Đề thi học kì 1 Hóa 8 năm 2020-2021]()
-
![Đề thi học kì 2 Hóa 8 trường PTDTBT THCS Liên xã La ÊÊ - Chơ Chun năm 2021-2022]()
Có thể bạn quan tâm
Thông tin tài liệu
PHÒNG GIÁO DỤC VÀ ĐÀO TẠO
Trường THCS Thái Bình
CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM
Độc lập –Tự do –Hạnh phúc
ĐỀ THI HỌC KÌ II NĂM HỌC 2018 – 2019
Môn thi: Hóa học ; LỚP: 8
Thời gian: 45 phút (không kể thời gian phát đề)
Câu 1(1,5đ):
a. Oxit là gì?
b. Cho các hợp chất vô cơ sau, hãy chỉ ra đâu là oxit, axit, bazơ, muối: Na 2O, H2S,
Zn(NO3)2, NaOH, CO2, H2SO4, Fe(OH)3, KHCO3.
Câu 2(1,5đ):
Hoàn thành các phản ứng hóa học sau và cho biết loại phản ứng của phương trình.
a.
KClO3
b.
Mg + HCl →
c.
Na2O + H2O →
Câu 3(2,5đ):
a. Thế nào là dung dịch, dung dịch bão hòa, dung dịch chưa bão hòa?
b. Hòa tan 40 gam NaOH vào 160 gam nước thì thu được dung dịch NaOH. Tính khối
lượng dung dịch NaOH tạo thành và nồng độ phần trăm của dung dịch.
Câu 4(1,5đ):
Có 3 lọ mất nhãn đựng 3 dung dịch không màu sau: axit clohiđric (HCl), Kali hiđroxit
(KOH), nước. Bằng phương pháp hóa học hãy nhận biết 3 lọ trên.
Câu 5(1đ): Đốt cháy 13 gam một kim loại R (hoá trị II) trong bình chứa khí oxi có dư, sau
phản ứng thu được 16,2 gam oxit RO. Xác định tên kim loại R.
Câu 6(2đ):
Cho 11,2 gam sắt (Fe) tác dụng vừa đủ với dung dịch axit sunfuric H 2SO4 10% thu được sắt
(II) sunfat (FeSO4) và giải phóng khí hiđro (H2).
a. Tính thể tích khí tạo thành ở điều kiện tiêu chuẩn.
b. Tính khối lượng dung dịch axit sunfuric cần dùng.
Cho biết nguyên tử khối của một số nguyên tố sau: Al = 27, O =16, Zn= 65, S= 32, Cl
=35,5, Ca = 40, H =1, Cu = 64, Fe= 56.
……………. Hết …………………..
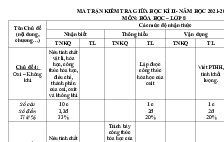
B. Ma trận đề kiểm tra học kì 2:
Nội dung kiến
thức
Chủ đề 1:
Oxi – không khí
Số câu:
Số điểm:
Chủ đề 2:
Hiđro – nước
Số câu
Số điểm
Chủ đề 3:
Dung dịch.
Số câu
Số điểm
Chủ đề 4:
Tổng hợp các nội
dung trên
Số câu
Số điểm
Tổng số câu
Tổng số điểm
Nhận biết
Thông hiểu
Oxit là gì?
1/2(Câu 1a)
0,5 đ
Chỉ ra chất
nào là oxit,
axit,
bazơ,
muối
1/2(Câu 1b)
1đ
Thế nào là
dung
dịch,
dung
dịch
bão
hòa,
dung
dịch
chưa
bão
hòa?
1/2(Câu 7)
1,5đ
1,5
3đ (30%)
Vận dụng
Cộng
Cấp độ thấp
Cấp độ cao
Áp dụng công
thức tính toán
hóa học làm
bài tập dạng
xác định tên
kim loại.
1 (Câu 5)
1,5
1đ
1,5đ (15%)
Nhận
biết
dung
dịch
bằng phương
pháp hóa học.
1(Câu 5)
1,5đ
1,5
2,5đ (25%)
Bài tập vận
dụng
tính
nồng
độ
dung dịch.
Hoàn
thành
các
phương
trình hóa học
sau và cho biết
loại phản ứng
của
phương
trình.
1 (Câu 2)
1,5đ
2
3đ(30%)
1/2(Câu 3)
1đ
Áp
dụng
công thức
tính
toán
hóa
học
làm bài tập
dạng 1 số
mol.
1(Câu 6)
2đ
1,5
1
3đ(30%)
1đ(10%)
1
2,5(25%)
2
3,5đ(35%)
6
10đ(100%)
C. ĐÁP ÁN VÀ HƯỚNG DẪN BIỂU ĐIỂM CHẤM:
Câu
Câu 1
(1,5đ)
Câu 2
(1,5đ)
Đáp án
Oxit là hợp chất của hai nguyên tố trong đó có một nguyên tố là oxi.
Oxit : Na2O, CO2.
Axit : H2S, H2SO4
Bazơ : NaOH, Fe(OH)3
Muối: Zn(NO3)2, KHCO3.
a. 2 KClO3
2KCl + 3O2
=> Phản ứng phân hủy
b. Fe + 2HCl →FeCl2 + H2
Biểu điểm
0,5đ
0,25đ
0,25đ
0,25đ
0,25đ
0,5đ
0,5đ
=> Phản ứng thế
c. Na2O + H2O → 2NaOH
=> Phản ứng hóa hợp
Câu 3 a. Dung dịch là hỗn hợp đồng nhất của dung môi và chất tan.
(2,5đ) - Dung dịch bão hoà là dung dịch không thể hoà tan thêm chất tan ở một
nhiệt độ xác định..
- Dung dịch chưa bão hoà là dung dịch có thể hoà tan thêm chất tan ở
một nhiệt độ xác định..
b.
- Khối lượng dung dịch NaOH tạo thành.
mdd = mct + mdm = 40 + 160 = 200 (gam)
0,5đ
0,5đ
0,5đ
0,5đ
0,5đ
0,5đ
- Nồng độ phần trăm của dung dịch NaOH là:
C% =
x100% =
x100% = 20%
Câu 4 Lấy 1 ít hóa chất để thử.
(1,5đ) Dùng quỳ tím để thử 3 dung dịch.
+ Qùy tím chuyển màu xanh. Đó là dung dịch KOH
+ Qùy tím chuyển màu đỏ. Đó là dung dịch HCl.
+ Không hiện tượng. Đó là nước.
Câu 5 PTHH : 2R + O2
2RO
(1đ)
Mol: 13g
16,2g
Theo định luật bảo toàn khối lượng, ta có:
mkhí oxi = mRO – mR = 16,2 – 13 = 3,2 gam
Số mol của khí oxi tham gia phản ứng là:
nkhí oxi =
=
= 0,1 (mol)
= 0,2 (mol)
= 65 (gam/mol)
Vậy R là kim loại kẽm.
Câu 6
(2đ)
=
0,25đ
= 0,4 (mol)
a. Theo PTHH, số mol của H2 là: nH2=
0,25đ
0,25đ
0,5đ
PTHH: Fe + H2SO4 → FeSO4 + H2
Mol 0,2
0,2
0,2
Số mol có trong 11,2 gam sắt.
nFe =
0,25đ
0,25đ
Theo PTHH, số mol của R là: nR=
Khối lượng mol của R là: MR=
0,75đ
0,25đ
0,25đ
0,25đ
= 0,2 (mol)
0,25đ
Thể tích của 0,2 mol khí hiđro tạo thành ở đktc là:
VH2= n. 22,4 = 0,2 .22,4 = 4,48 (l)
0,25đ
b. Theo PTHH, số mol của H2SO4: naxit=
0,25đ
Khối lượng của axit sunfuric cần dùng:
maxit = n. M= 0,2. 98 = 19,6 (gam)
Khối lượng của dung dịch axit cần dùng là:
mdd =
=
=196 (gam)
= 0,2 (mol)
0,25đ
0,25đ