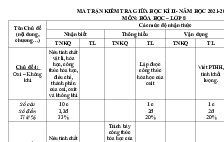
ĐỀ KIỂM TRA KỲ II MÔN HÓA HỌC LỚP 8
Nội dung tài liệu
Tải xuống
Link tài liệu:
Các tài liệu liên quan
-
![Đề thi học kì 1 Hóa 8 trường THCS TT Vĩnh Tường năm 2017-2018]()
-
![Đề kiểm tra học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa lớp 8 năm 2016-2017]()
-
![Đề thi học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Thái Bình năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Biên Giới năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Sơn Lâm năm 2021-2022]()
-
![Đề thi học kì 1 Hóa 8 năm 2020-2021]()
-
![Đề thi học kì 2 Hóa 8 trường PTDTBT THCS Liên xã La ÊÊ - Chơ Chun năm 2021-2022]()
Có thể bạn quan tâm
Thông tin tài liệu
BỘ 24 ĐỀ KIỂM TRA 1 TIẾT LẦN 2 HỌC KỲ 2 HÓA 8 TPHCM NĂM 2014-2015
ĐỀ SỐ 1: TRƯỜNG THCS TRẦN QUANG KHẢI, QUẬN TÂN PHÚ
Bài 1: (1,5 điểm) Bằng phương pháp hóa học hãy nhận biết các chất khí sau: H
2, O2, không khí.
Bài 2: (3 điểm) Hoàn thành các phương trình phản ứng và phân loại phản ứng:
1) Fe + H2SO4 ? + ?
3) ? + HCl AlCl3 + ?
9
t
P2O5 + H2O ?
4) KClO3
?+?
(1,5 điểm) Lập phương trình hóa học của các phản ứng sau:
Lưu huỳnh đioxit + nước axit sunfurơ (H2SO3)
Chì (II) oxit + hiđro chì + nước
Kẽm + axit clohiđric kẽm clorua + khí hiđro
(2,5 điểm) Cho 4,48 (l) khí hiđro (đktc) đi qua ống nghiệm chứa 23,3 (g) s ắt t ừ oxit.
Viết phương trình hóa học của phản ứng.
Sau phản ứng chất nào còn dư, dư bao nhiêu (g).
Tính khối lượng hơi nước thu được sau phản ứng.
(1,5 điểm) Hãy mô tả hiện tượng và viết phương trình minh họa cho thí nghiệm trên: đi ều chế khí
hiđro trong phòng thí nghiệm.
ĐỀ SỐ 2: TRƯỜNG THCS ĐẶNG TRẦN CÔN, QUẬN TÂN PHÚ
Bài 1: (1 điểm) Nêu hiện tượng xảy ra và viết phương trình hóa học khi dẫn khí H 2 qua bột CuO nung
nóng.
Bài 2: (3 điểm) Hoàn thành các phương trình phản ứng.
2)
Bài 3:
1)
2)
3)
Bài 4:
1)
2)
3)
Bài 5:
9
1) Na + H2O ? + ?
t
4) H2 + FeO
?+?
2) BaO + H2O ?
t
5) P + O2
?
3)
Bài 3:
Bài 4:
1)
9
9
t
SO3 + H2O ?
6) KClO3
?+?
(2 điểm) Phân loại và đọc tên các chất sau: NaOH, SO2, N2O5, Na2CO3.
(1 điểm) Cho biết các phản ứng sau thuộc loại phản ứng gì?
Al + HCl AlCl3 + H2
3) C + O2 CO2
9
t
2) Mg + CuCl2 MgCl2 + Cu
4) HgO
?+?
Bài 5: (3 điểm) Hòa tan 19,5 (g) kẽm Zn vào dung d ịch axit clohiđric HCl thu đ ược mu ối kẽm clorua ZnCl2
và khí hiđro H2.
1) Viết phương trình hóa học của phản ứng.
2) Tính thể tích khí hiđro thu được (đktc).
3) Tính khối lượng muối sinh ra.
4) Tính thể tích không khí (đktc) cần dùng để đốt cháy hết lượng khí hiđro ở trên.
ĐỂ DOWNLOAD ĐẦY ĐỦ TÀI LIỆU
SOẠN TIN: ENBIEN 945 gửi 7783
khoảng trắng