Đề kiểm tra giữa học kì 1 Hóa 8 tỉnh Quảng Nam năm 2020-2021
Nội dung tài liệu
Tải xuống
Link tài liệu:
Các tài liệu liên quan
-
![Đề thi học kì 1 Hóa 8 trường THCS TT Vĩnh Tường năm 2017-2018]()
-
![Đề kiểm tra học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa lớp 8 năm 2016-2017]()
-
![Đề thi học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Thái Bình năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Biên Giới năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Sơn Lâm năm 2021-2022]()
-
![Đề thi học kì 1 Hóa 8 năm 2020-2021]()
-
![Đề thi học kì 2 Hóa 8 trường PTDTBT THCS Liên xã La ÊÊ - Chơ Chun năm 2021-2022]()
Có thể bạn quan tâm
Thông tin tài liệu
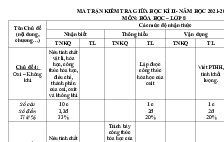
MA TRẬN ĐỀ KIỂM TRA GIỮA HỌC KỲ 1 NĂM HỌC 2020 – 2021
Môn: Hóa học – Lớp 8
Tên Chủ đề
Nhận biết
Thông hiểu
Vận dụng
Vận dụng cao
(nội dung,
chương…)
Chủ đề 1
Chất – đơn chất,
hợp chất
Số câu
Số điểm
Tỉ lệ %
Chủ đề 2
Nguyên tử phân tử nguyên tố hóa
học
Số câu
Số điểm
Tỉ lệ %
Chủ đề 3
Công thức hóa
học - Hóa trị .
Số câu
Số điểm
Tỉ lệ %
Chủ đề 4
Sự biến đổi chất.
Phản ứng hóa
học
Số câu
Số điểm
Tỉ lệ %
TNKQ
TL
- Khái niệm hóa học
- Chất và vật thể,
chất tinh khiết với
hỗn hợp
3
1đ
TNKQ
TL
TL
TNKQ
TL
Phân biệt đơn
chất và hợp chất
1
0,3đ
3%
10%
-Cấu tạo nguyên tử - Dựa vào NTK
-Phân tử
xác định tên
nguyên tố
-Nguyên tố hóa
-Tính được khối
học
lượng bằng gam
của 1 nguyên tử.
2
2
0,7đ
0,7đ
7%
7%
-Lấy hóa trị nguyên -Tính được PTK
tố nào làm đơn vị
của 1hợp chất,
hóa trị.
xác định được
-Ý nghĩa của
CTHH.
CTHH
-Tính hóa trị của
nguyên tố trong
hợp chất với Oxi
1
3
0,3đ
1đ
10%
3%
-Khái niệm và diễn
biến phản ứng hóa
học
TNKQ
Cộng
- Phân biệt các
HTVL, HTHH
- Diễn biến của
PƯHH
- Xác định chất
phản ứng, sản
phẩm
3
1đ
10%
4
1,3đ
13%
4
1,4đ
14%
-Lập CTHH của
hợp chất
2nguyên tố và 1
nguyên tố với
nhóm nguyên tử
-Tìm hóa trị của
1 nguyên tố
trong hợp chất
chưa biết chỉ số
nguyên tử
1
2đ
20%
1
1đ
10%
6
4,3đ
43%
4
3,0đ
20%
30%
6
1
1
18
Tổng số câu
1
9
2
Tổng số điểm
2
3
2
1
10đ
40%
Tỉ lệ %
30%
20%
10%
100%
(Kèm theo Công văn số 1749/SGDĐT-GDTrH ngày 13/10/2020 của Sở GDĐT Quảng Nam)
1
2đ
SỞ GIÁO DỤC & ĐÀO TAO
ĐỀ
CHÍNH NAM
THỨC
QUẢNG
(Đề có 02 trang)
ĐỀ KIỂM TRA GIỮA HỌC KÌ I – NĂM HỌC 2020-2021
MÔN: HÓA HỌC 8
Thời gian làm bài: 45 phút;
ĐỀ
I. TRẮC NGHIỆM:(5 điểm) Chọn phương án đúng.
Câu 1: Hóa học là gì?
A. Hoá học là khoa học nghiên cứu các chất, sự biến đổi chất.
B. Hoá học là khoa học nghiên cứu các môn học, sự tích hợp bộ môn.
C. Hoá học là khoa học nghiên cứu các sự vật và hiện tượng.
D. Hoá học là khoa học nghiên cứu các sự việc, sự vật và hiện tượng.
Câu 2: Trong các vật: Bút chì và cây xanh hãy cho biết đâu là vật thể tự nhiên và chất
A. cây xanh và bút chì.
B. cây xanh và chì.
C. bút chì và xelulozo.
D. bút chì và chì.
Câu 3: Chất nào là chất tinh khiết ?
A. Nước khoáng.
B.Nước biển.
C. Nước cất.
D. Nước suối
Câu 4: Chất thuộc hợp chất hóa học là:
A. O2.
B. N2.
C. H2.
D. CO2
Câu 5: Trong 1 phân tử nước H2O có các nguyên tử
A. 1 nguyên tử hiđrô và 2 nguyên tử oxi.
B. 2 nguyên tử hiđrô và 1 nguyên tử oxi
C. 1 nguyên tử hiđrô và 1 nguyên tử oxi.
D. 2 nguyên tử hiđrô và 2 nguyên tử oxi.
Câu 6: Nguyên tố hóa học là
A. Tập hợp các nguyên tử cùng loại.
B. Tập hợp các phân tử cùng loại.
C. Tập hợp các đơn chất cùng loại.
D. Tập hợp các chất cùng loại.
Câu 7: Nguyên tố X có nguyên tử khối bằng 3,5 lần nguyên tử khối của oxi. X là nguyên tố
nào sau đây?
A. Ca
B. Na
C. K
D. Fe
Câu 8: Khối lượng tính bằng gam của 1 nguyên tử Magie là:
A. 3,984.10-23g
B. 3,984g
C. 3,984.10-24đvc D.1,9926 đvC.
Câu 9: Hóa trị của một nguyên tố trong hợp chất cụ thể được xác định theo hóa trị của
A. H hóa trị I và O hóa trị II.
B. H hóa trị II và O hóa trị II.
C. H hóa trị I và O hóa trị I.
D. H hóa trị II và O hóa trị I.
Câu 10: Tính phân tử khối của 1 phân tử hợp chất CaCO3
A. 50đvC
B. 70đvC
C. 100đvC
D. 110đvC
Câu 11: Công thức hóa học của chất được tạo bởi Fe (II) và O là:
A. Fe2O2
B. Fe3O4
C. Fe2O3
D. FeO
Câu 12:Tính hóa trị của nguyên tố lưu huỳnh trong hợp chất với Oxi: SO2
A. II
B.III
C.IV
D.VI
Câu 13: Phân biệt các hiện tượng hóa học với hiện tượng vật lí là có
A. tạo chất rắn
B. tạo chất mới
C. tạo chất bay hơi
D. tạo chất khí
Câu 14: Phản ứng hóa học giữa phân tử oxi và phân tử hiđrô kết quả tạo ra sản phẩm là nước
có liên kết các nguyên tử nước là
A. 1 nguyên tử H liên kết với 1 nguyên tử O (HO).
B. 1 nguyên tử H liên kết với 2 nguyên tử O (HO2).
C. 2 nguyên tử H liên kết với 1 nguyên tử O (H2O) .
D. 2 nguyên tử H liên kết với 2 nguyên tử O (H2O2).
Câu 15: Xác định chất phản ứng và sản phẩm trong phản ứng sau: axit HCl tác dụng với
CaCO3 tạo ra CaCl2, nước và khí CO2
1. Chất phản ứng là: HCl và CaCO3
2. Sản phẩm là: CaCl2, nước và khí CO2
3. Chất phản ứng là: HCl, CaCO3 và CaCl2
4. Sản phẩm là: nước và khí CO2
A. 1,2,3,4 đúng
B. 1,2,3 đúng
C.1và 2 đúng
D. 3 và 4 đúng
II. TỰ LUẬN:(5 điểm)
Câu 16: (2đ) Phản ứng hóa học là gì? Trong phản ứng hóa học liên kết giữa các nguyên tử thay
đổi như thế nào? Kết quả của phản ứng hóa học như thế nào? Cho ví dụ minh họa?
Câu 17: (2đ) Lập công thức hóa học của hợp chất giữa nhôm(Al) hóa trị III với
a. O hóa trị II
b. Nhóm (SO4) hóa trị II
Câu 18: (1đ) Tìm hóa trị của nguyên tố Fe trong hợp chất với nhóm (OH) hóa trị I. Biết tỉ lệ
nguyên tử Fe với nhóm (OH) là 1:3
----------HẾT--------BÀI LÀM
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
.........................................................................................................................................................
ĐÁP ÁN-HƯỚNG DẪN CHẤM ĐIỂM
I. TRẮC NGHIỆM: (5điểm) Mỗi câu đúng 0,33 điểm, 3 câu đúng 1 điểm, 2 câu đúng 0,7
điểm
Câu
1 2 3 4 5 6 7
8 9 10 11 12 13 14 15
Đáp án A B C D B A D A A C
D
C
B
C
C
II. TỰ LUẬN: (5điểm)
Câ
Nội dung
Điểm
u
- Phản ứng hóa học là quá trình biến đổi chất này hành chất khác.
0,5
-Trong phản ứng hóa học chỉ có liên kết giữa các nguyên tử thay đổi làm cho 0,5
16 phân tử này biến đổi thành phân tử khác.
- Kết quả của phản ứng hóa học làm chất này biến đổi thành chất khác.
0,5
- Ví dụ: Đun nóng bột sắt với lưu huỳnh tạo ra chất mới là Sắt(II) sunfua
0,5
a.AlxOy Quy tắc hóa trị x:y=II:III suy ra x=II, y=III Vậy CTHH là: Al2O3
1
17
b.Alx(SO4)y: Quy tắc hóa trị x:y=II:III suy ra x=II, y=III Vậy CTHH là: Al2(SO4)3
1
- Fex(OH)y Ta có x:y=1:3 suy ra x=1, y=3 Vậy CTHH là: Fe(OH) 3 áp dụng quy
18
1
tắc hóa trị ta tính được hóa trị của Fe là: 1.a=3.I suy ra a=III