Lý thuyết và Phương pháp giải
Bài toán 1: SO2 + NaOH hoặc KOH
SO2 + NaOH → NaHSO3 (1)
SO2 + 2NaOH → Na2SO3 + H2O (2)
Lập tỉ lệ T = nNaOH / nSO2
T ≤ 1 → chỉ xảy ra phản ứng (1) tức tạo muối NaHSO3 (muối axit)
1 < T < 2 → xảy ra cả (1) và (2) tức tạo 2 muối NaHSO3 và Na2SO3
T ≥ 2 → chỉ xảy ra phản ứng (2) tức tạo muối Na2SO3 (muối trung hòa)
Bài toán 2: SO2 + Ba(OH)2 /Ca(OH)2
SO2 + Ba(OH)2 → BaSO3↓ + H2O (1)
2SO2 + Ba(OH)2 → Ba(HSO3)2 (2)
Lập tỉ lệ T = nSO2 / nBa(OH)2
T ≤ 1 → chỉ xảy ra phản ứng (1) tức tạo muối BaSO3 ↓
1 < T < 2 → xảy ra cả (1) và (2) tức tạo 2 muối BaSO3 ↓ và Ba(HSO3)2
T ≥ 2 → chỉ xảy ra phản ứng (2) tức tạo muối Ba(HSO3)2 (muối tan, không tạo kết tủa)
Ví dụ minh họa
Ví dụ 1 : Hấp thụ 3,36 lít khí SO2 (đktc) vào 200 ml dung dịch NaOH aM. Tính a biết sau phản ứng chỉ thu được muối trung hòa.
Hướng dẫn:
Vì đề cho chỉ tạo muối trung hòa nên chỉ xảy ra phản ứng
SO2 + 2NaOH → Na2SO3 + H2O
0,15 → 0,3
nSO2 = 0,15 mol , VNaOH = 200 ml = 0,2 lít
→ a = CMNaOH = 0,15/0,2 = 0,75M
Ví dụ 2: Hấp thụ hoàn toàn 12,8g SO2 vào 250 ml dung dịch NaOH 1M. Tính khối lượng muối tạo thành sau phản ứng.
Hướng dẫn:
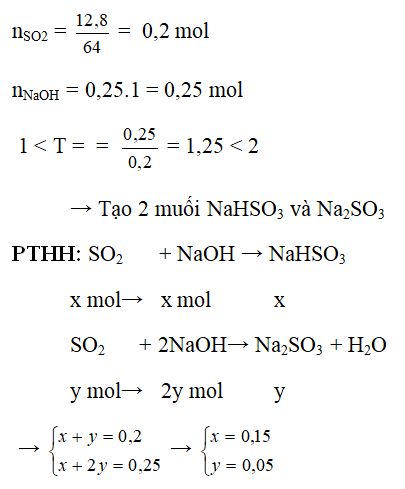
→ mNaHSO3 = 0,15. 104 = 15,6g
mNa2SO3 = 0,05 . 126 = 6,3g
Nhận xét : Có thể nhẩm nhanh trắc nghiệm: số mol 2 muối = số mol SO2
nNa2SO3 = nNaOH - nSO2 = 0,25 – 0,2 = 0,05 mol
nNaHSO3 = nSO2 - nNa2SO3 = 0,2 – 0,05 = 0,15 mol
Ví dụ 3: Hấp thụ 6,72 lít khí SO2 (đktc) vào 100 ml dung dịch Ba(OH)2 2M. Tính khối lượng muối thu được
Hướng dẫn:

Cách 2: Ba(OH)2 + SO2 → BaSO3↓ + H2O
x mol → x mol → x mol
BaSO3 + SO2dư + H2O → Ba(HSO3)2
x mol → x mol
tạo kết tủa, khi dư SO2, kết tủa bị hòa tan, để hòa tan hết kết tủa nSO2 ít nhất = 2x= 2nBa(OH)2
Nếu lượng SO2 không đủ để hòa tan hết kết tủa, thì kết tủa chỉ bị tan một phần tức tồn tại 2 muối BaSO3 và Ba(HSO3)2
Ba(OH)2 + SO2 → BaSO3↓ + H2O
0,2 → 0,2 0,2
BaSO3 + SO2dư + H2O → Ba(HSO3)2
0,1 ← (0,3-0,2) → 0,1
nBaSO3 còn lại = 0,2 – 0,1 = 0,1 mol
Cách 3: Nhẩm trắc nghiệm: để hòa tan hết kết tủa nSO2 = 2nBa(OH)2 , nếu lượng kết tủa chỉ bị tan một phần
nSO2 = 2nBa(OH)2 - nkết tủa (vì tỉ lệ số mol hòa tan kết tủa là 1:1)
→ nBaSO3 còn lại = 2nBa(OH)2 - nSO2 = 2.0,2 – 0,3 = 0,1 mol
Số mol 2 muối = số mol Ba(OH)2 → nBa(HSO3)2 = nBa(OH)2 - nBaSO3 còn lại = 0,2 – 0,1 = 0,1 mol
→ mBaSO3 = 0,1 . 217 = 12,7g
mBa(HSO3)2 = 0,1.299 = 29,9g
Ví dụ 4: Dẫn khí SO2 qua 200 ml dung dịch Ba(OH)2 aM thu được 21,7 g kết tủa, thêm tiếp dung dịch NaOH đến dư vào lại thu thêm 10,85 gam kết tủa nữa. Tính a
Hướng dẫn:
Thêm NaOH lại thu thêm kết tủa, chứng tỏ trong dung dịch tồn tại muối Ba(HSO3)2, mà vẫn có kết tủa
→ tồn tại 2 muối
n↓(1) = 21,7/217 = 0,1 mol
n↓(2) = 10,85/217 = 0,05 mol
Ba(OH)2 + SO2 → BaSO3 ↓+ H2O
0,1 0,1
Ba(OH)2 + 2SO2 → Ba(HSO3)2
0,05 ← 0,05
Ba(HSO3)2 + 2NaOH → BaSO3 ↓ + Na2SO3 + 2H2O
0,05 ← 0,05
nBa(OH)2 = 0,1 + 0,05 = 0,15 mol → a = = 0,75M
Cách 2: ∑n↓ = 0,1 + 0,05 = 0,15 mol
Ba(OH)2 → BaSO3
0,15 ← 0,15
→ a = 0,15/0,2 = 0,75M
Được cập nhật: 24 tháng 4 lúc 2:26:13 | Lượt xem: 766




